چکیده
ملاسمیا یک بیماری شایع هیپرپیگمانتاسیون است که به دلیل شباهتش به اختلالات ناشی از پیری پوست ناشی از تابش نور، درمان آن چالشبرانگیز است. مطالعات متعددی به ماهیت پیچیده ملاسمیا پرداختهاند که اغلب شباهتهایی به اختلالات پیری ناشی از تابش نور دارد. رویکردهای درمانی مختلفی شامل درمانهای موضعی و سیستمیک، لایهبرداری شیمیایی و درمان با لیزر در تحقیقات گذشته نشان دادهاند که در مدیریت ملاسمیا مؤثر هستند. با این حال، ملاسمیا حتی پس از درمان موفق بهطور مکرر بازمیگردد که عمدتاً به دلیل ویژگیهای ذاتی پیری ناشی از تابش نور آن است. از آنجا که ملاسمیا ویژگیهایی مشابه با اختلالات پیری ناشی از تابش نور دارد، از جمله اختلالات در غشای پایه، الاستوزیس خورشیدی، آنژیوجنزیس و نفوذ سلولهای ماست در لایه درم، یک استراتژی درمانی جامع ضروری است. چنین رویکردی ممکن است شامل مقابله با هایپرپیگمانتاسیون اپیدرمی در حالی که اجزای درم را نیز بازسازی میکند باشد. در این مقاله، ما یک مرور جامع از روشهای درمانی مرسوم که بهطور رایج در عمل بالینی استفاده میشوند، همچنین درمانهای نوآورانهای که در حال توسعه هستند برای مدیریت ملاسمیا ارائه میدهیم. علاوه بر این، یک نمای کلی وسیع از پاتوژنز ملاسمیا نیز ارائه میدهیم.
کلمات کلیدی: ملانوز؛ ملاسمیا؛ پاتولوژی؛ پیری پوست؛ درمان
مقدمه
ملاسمیا یک اختلال شایع هایپرپیگمانتاسیون است که با لکهها و لکههای نامنظم و غیرقرینه با مرزهای نامنظم از رنگ قهوهای روشن تا تیره در نواحی در معرض آفتاب مشخص میشود. این بیماری معمولاً زنان را در دهههای سوم یا چهارم زندگی با انواع پوست فیتزپاتریک III-IV تحت تأثیر قرار میدهد. مهمترین عوامل علتشناسی ملاسمیا، آسیبپذیری ژنتیکی، هورمونهای جنسی و تابش اشعه ماوراء بنفش (UV) است. ملاسمیا معمولاً به درمانهای رایج مقاوم است و اغلب حتی پس از درمان موفق مجدداً عود میکند. برای درک چالشهای درمان ملاسمیا، ضروری است که پاتوفیزیولوژی آن را درک کنیم. چندین مطالعه اخیر موجب بهروزرسانی درک ما از ملاسمیا شدهاند.
پاتوژنز ملاسمیا
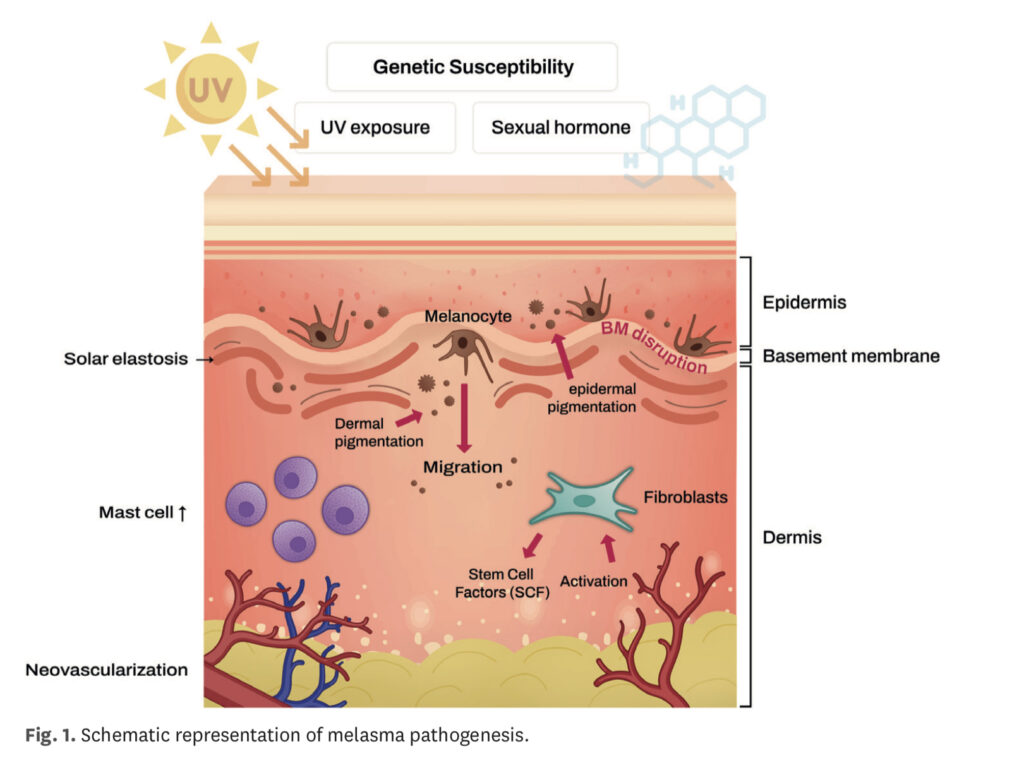
پیشتر ملاسمیا به عنوان یک اختلال در ملانوسیتها شناخته میشد. با این حال، مطالعات اخیر نقش اجزای درم مانند سلولهای ماست، الاستوزیس خورشیدی و نئووسکولاریزاسیون را در پاتوژنز ملاسمیا همراه با ملانوسیتها درک کردهاند. زمانی که تابش UV تجمع مییابد، التهاب مزمن درم رخ میدهد که موجب فعال شدن فیبروبلاستها میشود. سپس، فیبروبلاستهای تابشدیده از UV فاکتور سلولهای بنیادی (SCF) را ترشح میکنند که از طریق سیگنالدهی با گیرنده خود، c-kit، در اپیدرم، موجب ملانوژنز میشود. علاوه بر این، فیبروبلاستهای سالمند در پوست مبتلا به ملاسمیا نسبت به پوست سالم پیرامون آن افزایش یافتهاند. فیبروبلاستهای سالمند به تولید پروتئینهای بیشتری که به پیری پوست مرتبط هستند، مانند SCF، معروف هستند. همچنین در پوست مبتلا به ملاسمیا، افزایش تنظیمکنندههای مرتبط با سیگنالدهی Wnt مشاهده میشود. علاوه بر این، کاهش بیان فاکتور مهارکننده Wnt-1 (WIF-1) در پوست هیپرپیگمانته مبتلا به ملاسمیا مشاهده شده است.
کاهش تنظیم WIF-1 که میتواند در کراتینوسیتهای اپیدرمی و فیبروبلاستهای درم رخ دهد، به توسعه ملاسمیا ارتباط داده شده است، زیرا نقش آن در تحریک ملانوژنز و انتقال ملانوزومها از طریق افزایش هر دو مسیر سیگنالدهی وینت کانونیکال و غیرکانونیکال است. در عین حال، آزادسازی پروتئین مربوط به فریزلد 2 (FRP2) به عنوان یک محرک برای ملانوژنز از طریق فعالسازی مسیر سیگنالدهی β-کاتنین عمل میکند. علاوه بر این، سیکلوکسیژناز-2 (COX-2) ناشی از UV برای تحریک بیشتر ملانوسیتها شناخته شده است.
در پوست مبتلا به ملاسمیا، ملانوسیتهای معلق به درم افتادهاند که ویژگی این بیماری است و ملانوفاجهای درم مشاهده شدهاند. محتوای ملانین در درم به احتمال زیاد توسط اختلال در غشای پایه تقویت میشود. با استفاده از رنگآمیزی اسید پرودییک-شِیف-دیاستاز (D-PAS) و ایمنوهیستوشیمی ضد کلاژن نوع IV، 95.5% و 83% از نمونههای پوستی از بیماران مبتلا به ملاسمیا با انواع پوست فیتزپاتریک IV و V به ترتیب نشاندهنده اختلال در غشای پایه بودند.
تابش مزمن UV، متالوپروتئینازها (MMP2) و MMP9 را فعال میکند تا کلاژن نوع IV و VI در غشای پایه را تجزیه کند. سقوط ملانوسیتها و ملانین در درم، تسهیلشده توسط غشای پایه، موجب میشود که ملاسمیا مقاوم به درمانهایی باشد که به رنگدانههای اپیدرمی هدف دارند.
سلولهای ماست بیشتر در پوست مبتلا به ملاسمیا نسبت به پوست سالم مشاهده میشوند. تابش UV به نظر میرسد که باعث آزادسازی هیستامین از سلولهای ماست درم میشود. نقش هیستامین در ملانوژنز هنوز مشخص نیست، اما گفته میشود که با فاکتور رشد-تمایزیابی 15 (GDF-15) که از خانواده فاکتورهای رشد تحولزا (TGF-β) است، ارتباط دارد. همچنین هیستامین شناخته شده است که از طریق فعالسازی پروتئین کیناز A از طریق گیرندههای H2، سلولهای ملانوسیت انسانی را تحریک میکند. علاوه بر این، تابش UV مزمن باعث افزایش تریپتاز آزاد شده توسط سلولهای ماست میشود. تریپتاز آزاد شده از سلولهای ماست باعث تجزیه کلاژن نوع IV از طریق فعالسازی اشکال غیرفعال MMPها یا آسیب مستقیم به اجزای ماتریکس خارجسلولی (ECM) میشود. بنابراین، افزایش تریپتاز آزاد شده توسط سلولهای ماست میتواند اختلالات سلولی پایه در بیماران مبتلا به ملاسمیا را القا کند.
علاوه بر این، سلولهای ماست فاکتورهای متنوعی را که مرتبط با آنژیوژنز هستند، از جمله فاکتور رشد فیبروبلاست پایه (bFGF)، فاکتور رشد اندوتلیال عروقی (VEGF) و TGF-β را آزاد میکنند.
علاوه بر این، تابش UV طولانیمدت منجر به توسعه الاستوزیس خورشیدی میشود که با تجمع غیرطبیعی بافت الاستیک در درم مشخص میشود، پدیدهای که به طور معمول در پوست مبتلا به ملاسمیا مشاهده میشود. پیشنهاد شده است که تریپتاز ترشحشده از سلولهای ماست در ایجاد الاستوزیس خورشیدی نقش دارد، زیرا فیبروبلاستها را برای تولید الاستین تحریک میکند. همچنین، گرانزیم B که توسط سلولهای ماست ترشح میشود، شناخته شده است که پس از تابش UV طولانیمدت به تجزیه ECM کمک میکند.
مطالعات قبلی گزارش دادهاند که تعداد و اندازه رگهای خونی در پوست مبتلا به ملاسمیا به طور قابل توجهی افزایش یافته است. در داخل این رگهای خونی تغییر یافته، افزایش بیان VEGF مشاهده شده است. VEGF شناخته شده است که باعث آزادسازی اسید آراشیدونیک و فسفریلاسیون و فعالسازی فسفولیپاز A2 سیتوزولی میشود. اگرچه مکانیزم دقیق هنوز روشن نیست، پیشنهاد میشود که VEGF ممکن است ملانوژنز را از طریق افزایش بیان گیرنده-2 فعالشده توسط پروتئاز (PAR-2) القا کند. علاوه بر این، آندوتلین 1 که توسط سلولهای اندوتلیال میکروواسکولاری تولید میشود، شناخته شده است که باعث تحریک ملانوژنز میشود. این کار را از طریق فعالسازی فاکتور رونویسی مرتبط با میکروفتالمی (MITF) از طریق فعالسازی گیرنده آندوتلین B انجام میدهد.
بر اساس دانش انباشتهشده، واضح است که ملاسمیا تنها یک اختلال هایپرپیگمانتاسیون اپیدرمی نیست؛ بلکه یک وضعیت پیچیده است که ویژگیهایی مشابه اختلالات پیری ناشی از تابش نور دارد (شکل 1). این عوامل درمان ملاسمیا را به چالش کشیده و انجام درمان مؤثر را دشوار میسازد. برای مقابله با این مشکلات، تلاشهای تحقیقاتی به سمت توسعه درمانهایی که بر فیزیولوژی پاتولوژیک زمینهای ملاسمیا تمرکز دارند.
کرم ضد آفتاب
طیف طولموج تابش خورشیدی به سه بخش مادون قرمز (780–5000 نانومتر)، نور مرئی (VL) (400–780 نانومتر) و اشعه ماوراء بنفش (UV) (290–400 نانومتر) تقسیم میشود. بهخوبی شناخته شده است که هم تابش UV و هم تابش نور مرئی باعث تغییرات رنگدانهای میشوند، که از طریق مکانیسم فیزیولوژیکی توضیح داده میشود، جایی که تولید گونههای واکنشی اکسیژن (ROS) منجر به آزادسازی سیتوکینهای التهابی و آنزیمهای تخریبکننده ماتریکس در پوست میشود. یک مطالعه اخیر همچنین نشان داد که نور مرئی باعث هیپرپیگمانتاسیون طولانیمدت از طریق فعالسازی فاکتور رونویسی مرتبط با میکروفتالمی وابسته به کلسیم و تنظیمشده توسط اوپسین 3 میشود. با توجه به این یافته، حفاظت از پوست در برابر نور مرئی برای بیماران مبتلا به ملاسمیا مهم است. در واقع، کاستانیدو-کازارس و همکارانش ۶۸ بیمار مبتلا به ملاسمیا را به دو گروه تقسیم کردند تا بهطور تصادفی کرم ضد آفتاب UV-VL یا ضد آفتاب UV فقط دریافت کنند. در هفته هشتم، گروه اول نسبت به گروه دوم به ترتیب ۱۵٪، ۲۸٪ و ۴٪ بهبود بیشتر در نمرات شاخص ناحیه و شدت ملاسمیا (MASI)، مقادیر رنگسنجی و ارزیابی ملانین نشان داد. بهطور مشابه، بوکاری و همکاران یک مطالعه کنترلشده تصادفی دیگر طراحی کردند که دو گروه ضد آفتاب را مقایسه میکرد که در آنها یکی از گروهها حاوی اکسید آهن، یک رنگدانه جذبکننده نور مرئی بود. نویسندگان گزارش دادند که در گروه اکسید آهن در ۶ ماه، نمره MASI بهطور معناداری پایینتر بود. با توجه به این شواهد متقاطع، استفاده از کرم ضد آفتاب حاوی اکسید آهن یا تیتانیوم دیاکسید و زینک اکسید با اندازه ذرات بزرگتر از ۲۰۰ نانومتر، علیرغم مشکلات ظاهری ناشی از کدرشدن سفید، بهطور قوی توصیه میشود.
درمانهای موضعی
۱) عاملهای روشنکننده پوست
عاملهای روشنکننده پوست موضعی در درمان ملاسمیا رایج هستند. این ترکیبات هدفگذاری میکنند روی تیروزیناز، آنزیم محدودکننده سرعت در مسیر ملانوژنز. هیدروکینون، یکی از مهارکنندههای تیروزیناز، برای دههها بهعنوان معیار در درمان هایپرپیگمانتاسیون تثبیت شده است. فرضیه بر این است که هیدروکینون با اتصال به آنزیم یا تعامل با مولکول مس در سایت فعال آنزیم، تیروزیناز را مهار میکند. این باعث کاهش تشکیل ملانوزومها، تغییرات قابلتوجه در ساختار داخلی ملانوزوم، افزایش تجزیه ملانوزومها و در نهایت، تخریب اندامکهای غشایی در ملانوسیتها میشود. همراه با این مکانیسم زیرین، در واقع هیدروکینون باعث کاهش وابسته به دوز در پیگمانتاسیون در معاینات بالینی شد، جایی که آن را بهطور موضعی بر پشت دستها با لنتیگینهای خورشیدی در غلظتهای مختلف (۲٪، ۳٪ و ۵٪) اعمال کردند. مطالعات بیشتر نیز اثرات روشنکنندگی پوست آن را پیشنهاد کردند. انِس و همکاران نسبت پاسخ کامل بالینی در گروههای بیماران مبتلا به ملاسمیا که کرم هیدروکینون ۴٪ و دارونما استفاده میکردند را مقایسه کردند. محققان دریافتند که بین دو گروه تفاوت قابل توجهی وجود دارد (۳۸٪ در مقابل ۸٪). با وجود این شواهد انباشته که اثربخشی آن را تضمین میکند، مسائل ایمنی به طور مداوم مطرح شده است و اغلب باعث تردید در استفاده از آن میشود. به عنوان مثال، نگرانیها در مورد جذب سیستمیک دارو و کارسینوژنز القا شده توسط دارو مطرح شده است. نگرانیهای دیگر نیز مطرح شده که چندین گزارش از آکرونوز اگزودنوس به احتمال زیاد به دلیل استفاده از هیدروکینون بوده است.
۲) رتینوئیدهای موضعی
رتینوئیدهای موضعی اثربخشی خود را در درمان ملاسمیا نشان دادهاند. اعتقاد بر این است که رتینوئیدها موجب تحریک چرخش کراتینوسیتها، مهار انتقال ملانوزومها و اجازهدهی به نفوذ دیگر درمانهای موضعی از طریق اپیدرم میشوند. در مقایسه کرم ترتینوئین ۰.۱٪ با دارونما در مدت زمان ۴۰ هفته، گریفیثس و همکاران دریافتند که ۶۸٪ از گروه درمانی در ارزیابیهای رنگسنجی و هیستولوژیک بهبود نشان دادند، در حالی که تنها ۵٪ از گروه دارونما بهبود نشان دادند. قابلتوجه است که اثرات این درمان تا ۲۴ هفته واضح نبود و بسیاری از بیماران درمانشده (۸۸٪) عوارض جانبی از جمله اریتم و پوستریزی را تجربه کردند. با توجه به طولانیبودن زمان درمان مورد نیاز برای دستیابی به مزایای بالینی و بروز شایع تحریک، ترتینوئین ممکن است گزینه درمانی مناسب بهعنوان درمان تکدارویی نباشد.
۳) ترکیبهای موضعی
کرم ترکیب سهگانه (TCC)، شامل هیدروکینون، رتینوئید و کورتیکواستروئید موضعی، بهطور گستردهای برای درمان ملاسمیا استفاده میشود. تیلور و همکاران اثربخشی بالای آن را در مقایسه با هر ترکیب دوتایی از سه ماده فعال در یک مطالعه کنترلشده تصادفی بزرگ و چندمرکزی نشان دادند. ۷۷٪ از شرکتکنندگانی که از TCC استفاده کرده بودند، به بهبودی کامل یا تقریباً کامل رسیدند، در حالی که تنها ۴۷٪ از گروه ترکیب دوتایی به این نقطه دست یافتند. فریرا سِستاری و همکاران همچنین برتری آن را نسبت به هیدروکینون ۴٪ از نظر اثربخشی نشان دادند. پاکسازی ملاسمیا، به معنای نواحی تقریباً معادل با پوست پیرامونی، در ۳۵٪ از افرادی که از TCC استفاده کرده بودند مشاهده شد، در حالی که تنها ۵٪ از افرادی که فقط هیدروکینون استفاده کرده بودند به این نتیجه رسیدند.
یکی از فرضیهها اثرات همافزای ترکیبات این محصول را توضیح میدهد. به طور خاص، استروئید موضعی تصور میشود که تحریک ناشی از دو ترکیب دیگر را تسکین میدهد و سنتز ملانین را مهار میکند، در حالی که رتینوئید به اعتقاد بر این است که اکسیداسیون هیدروکینون را قطع کرده و نفوذ آن به اپیدرم را تسهیل میکند. با توجه به اینکه هیدروکینون در غلظتهای بالای ۴٪ و در دورههای درمانی بیش از ۳ ماه ممکن است با شروع جدید اوکرونوز همراه باشد، فرمول ترکیبی که غلظت هیدروکینون را به ۴٪ محدود میکند به دلیل اثرات ترکیبی با دیگر اجزای تشکیلدهنده میتواند توضیحدهنده خطر کمتر اوکرونوز باشد.
۴) روشهای درمانی تحقیقاتی
از آنجایی که تلاشهای علمی مکانیزمهای فیزیولوژیک مربوط به شروع و پیشرفت ملاسمیا را آشکار کردهاند، عوامل موضعی مختلفی که هر مرحله از هایپرپیگمنتیشن پوستی را هدف قرار میدهند، پیشنهاد شده است.
کرم شبیهسازی سیآرانآی (MITF-siRNA) به طور مؤثری هیپرملانوزیس صورت قهوهای و پوست معمولی را در افراد آسیایی روشن کرده است، با مهار مسیر تیروسیناز.
مهارکنندههای پمپ پروتون موضعی (PPI) مانند امپرازول نیز ممکن است ملانوژنز را مهار کنند و درمانی امیدوارکننده برای ملاسمیا به حساب آیند. امپرازول که به طور موضعی بر روی پوست افراد تحت تابش UV اعمال شده است، پس از ۳ هفته کاهش قابل توجهی در سطح پیگمنتها نسبت به گروههای کنترل بدون درمان ایجاد کرده است. این فرضیه وجود دارد که امپرازول با مهار ATP7A و تقویت تخریب تیروسیناز، ملانوژنز را کاهش میدهد. در کنار این یافته، همچنین قابل توجه است که PPIها ممکن است باعث تحریک یا بدتر شدن ویتیلیگو شوند، که از طریق گزارشهای بالینی مشاهده شده است که در آن بیماران پس از استفاده از PPIهای خوراکی دچار عود یا توسعه ویتیلیگو شدهاند.
متیمازول یک داروی ضد تیروئید خوراکی است که معمولاً برای درمان پرکاری تیروئید استفاده میشود. قابل توجه است که کاربرد موضعی متیمازول باعث کاهش پیگمنتاسیون میشود، بنابراین میتوان از آن برای درمان بیماران مبتلا به ملاسمیا و هایپرپیگمنتاسیون پس از التهاب (PIH) استفاده کرد. این طور تصور میشود که متیمازول با مهار پراکسیداز، سنتز ملانین را مسدود میکند.
درمانهای سیستمی
۱) اسید ترانکزامیک خوراکی (TXA)
TXA که به طور اصلی برای خواص هموستاتیک خود طراحی شده است، به عنوان یک عامل ضد فیبرینولیتیک عمل میکند. با دخالت در سیستم پلاسمینوژن/پلاسمین، TXA ارتباط بین کراتینوسیتها و ملانوسیتها را تحت تأثیر قرار میدهد. علاوه بر این، TXA فعالیت پلاسمین ناشی از تابش UV را مهار کرده و باعث کاهش فعالیت سلولهای ماست و مهار عامل رشد فیبروبلاست میشود.
این، به نوبه خود، منجر به کاهش تعداد سلولهای ماست در درم و کاهش تشکیل رگهای خونی جدید میشود. علاوه بر این، یک مطالعه جدید پیشنهاد کرده است که TXA میتواند سیستم اتوفاژی را از طریق افزایش بیان پروتئینهای مرتبط با اتوفاژی فعال کند. تحقیقات قبلی نشان میدهند که سیستم اتوفاژی نقش مهمی در تعیین رنگ پوست ایفا میکند.
مطالعات متعددی در مورد دوز مناسب TXA انجام شده است.
– کرن و همکاران نشان دادند که گروهی که ۵۰۰ میلیگرم TXA روزانه را علاوه بر درمانهای موضعی (هیدروکینون موضعی با ضد آفتاب) دریافت کردند، نسبت به گروهی که فقط درمانهای موضعی دریافت کردند، پس از ۱۲ هفته بهبودی در نمرات MASI داشتند.
– یونیس و همکاران کاهش ۴۹٪ در شاخص شدت و وسعت ملاسمیا (mMASI) را در گروهی که به مدت سه ماه ۵۰۰ میلیگرم TXA روزانه دریافت کردند، نشان دادند.
– میننی و همکاران نشان دادند که در گروهی که ۵۰۰ میلیگرم TXA روزانه به همراه کرم ترکیبی سهگانه دریافت کردند، ۶۵.۶٪ از بیماران بهبودی ۷۵٪ یا بیشتر را در ۱۲ هفته تجربه کردند، در حالی که فقط ۲۷.۱٪ در گروه درمان فقط موضعی این سطح از بهبودی را به دست آوردند.
در مطالعهای که توسط ژو و همکاران انجام شد، افرادی که به طور تصادفی به دوزهای مختلف TXA (۵۰۰ میلیگرم، ۷۵۰ میلیگرم، ۱۰۰۰ میلیگرم یا ۱۵۰۰ میلیگرم) اختصاص داده شده بودند، هیچ تفاوت معنیداری در نمرات MASI یا شاخص ملانین بین گروههای مختلف دوز مشاهده نکردند، اگرچه نتایج سریعتری با دوزهای بالاتر به دست آمد.
با افزایش استفاده از درمانهای مبتنی بر نور یا لیزر برای ملاسمیا، چندین مطالعه در مورد استفاده از TXA خوراکی همراه با درمانهای لیزری انجام شده است. مطالعهای که توسط چو و همکاران انجام شد، کاهش قابل توجهتری در نمرات mMASI در گروهی که درمان ترکیبی شامل ۵۰۰ میلیگرم TXA به همراه نور پالس شدید (IPL) و لیزر QS Nd:YAG با فلونس پایین دریافت کردند، گزارش کرده است.
در نهایت، شین و همکاران نشان دادند که درمان ترکیبی ۷۵۰ میلیگرم TXA با لیزر QS Nd:YAG با فلونس پایین باعث کاهش بیشتری در نمره میانگین mMASI در هشت هفته پس از درمان نسبت به درمان با لیزر تنها شد.
نگرانیهایی درباره خطر ترومبوز ناشی از استفاده از TXA به عنوان یک عامل هموستاتیک وجود دارد. با این حال، این خطر در بزرگسالان جوان بدون شرایط پزشکی زمینهای و افرادی که داروهای دیگر مصرف نمیکنند، بسیار کم است. با این حال، ضروری است که غربالگری جامع برای افرادی که عوامل خطر ترومبوآمبولی اضافی دارند، از جمله افرادی که بیماری قلبی عروقی دارند و تحت درمان با داروهای ضد انعقاد هستند، انجام شود. این افراد باید برای درمان سیستمی TXA منع شوند.
با وجود پروفایل ایمنی نسبتاً خوب TXA خوراکی، تلاشهایی برای بررسی روشهای مختلف تحویل این دارو انجام شده است. TXA موضعی در فرمولاسیونهای مختلفی مانند ژل یا محلول مورد تحقیق قرار گرفته است. علاوه بر این، برای افزایش اثربخشی TXA موضعی، چندین استراتژی برای ارتقای تحویل آن به کار گرفته شده است، از جمله میکرونیدلینگ یا تکنیکهای لیزر فرکشنال CO2. علاوه بر این، میکرواینژکشن درمیک TXA نیز در مطالعات قبلی اثربخش ثابت شده است.
۲) سایر عوامل سیستمی
**پولایپودیوم لوکوتوموس (PL)** یک سرخس استوایی است که از مناطق مرکزی و جنوبی آفریقا originates. PL به دلیل اثرات آنتیاکسیدانی، ضد التهابی و همچنین اثرات فتوپروتکتیو شناخته شده است که با اسکن کردن چندین ROS و مهار تشکیل پراکسیداسیون چربی عمل میکند. چندین تلاش برای استفاده از PLE خوراکی برای درمان ملاسمیا صورت گرفته است، اما نتایج به طور قطع غیرقطعی بوده است.
سایر عوامل سیستمی که برای درمان ملاسمیا مورد مطالعه قرار گرفتهاند شامل ویتامین C، ویتامین E، عصاره غنی از پروآنتوسیانیدین از دانههای انگور، جینسنگ قرمز کرهای، کاروتنوئیدها یا عصاره پوست درخت کاج دریایی فرانسه هستند. اگرچه نشان داده شده است که این مواد اثرات مفید و امیدوارکنندهای در درمان ملاسمیا به دلیل اثرات آنتیاکسیدانی دارند، شواهد کافی برای پشتیبانی از استفاده از آنها محدود است و تحقیقات بیشتری مورد نیاز است.
لایهبرداری شیمیایی
لایهبرداری شیمیایی یک گزینه درمانی شناخته شده برای ملاسمیا است و معمولاً به عنوان رویکرد ثانویه در مدیریت این وضعیت در نظر گرفته میشود. اثربخشی آنها در مقابله با بخش اپیدرمی ملاسمیا به توانایی آنها در ایجاد جداسازی کنترلشده اپیدرمی و سپس بازسازی نسبت داده میشود. علاوه بر این، آنها ممکن است به حذف ملانین ایستا از طریق فاگوسیتوز در لایههای درم کمک کنند. با این حال، باید توجه داشت که لایهبرداری شیمیایی دارای خطر قابل توجهی از ایجاد PIH است، به ویژه در افرادی که نوع پوست فیتزپاتریک III تا VI دارند.
۱) لایهبرداری با اسید گلیکولیک (GA)
لایهبرداری GA شایعترین لایهبرداری α-هیدروکسی است که کوچکترین وزن مولکولی را دارد و به راحتی وارد اپیدرم میشود. چندین مطالعه اثربخشی لایهبرداریهای GA را بررسی کردهاند. با این حال، بیشتر آنها برتری خاصی نسبت به درمانهای موضعی نشان ندادهاند. در یک مطالعه تقسیم صورت که توسط Lim و Tham انجام شد، آنها یک رویکرد ترکیبی (لایهبرداری GA ۲۰%–۷۰% هر سه هفته یکبار و یک محصول موضعی حاوی ۱۰% GA و ۲% HQ) را با درمان فقط موضعی مقایسه کردند. نتایج نشان داد که هیچ تفاوت معنیداری بین دو طرف وجود نداشت. به طور مشابه، در یک مطالعه دیگر که توسط Hurley و همکاران انجام شد، بیماران لایهبرداری GA ۲۰%–۳۰% هر دو هفته یکبار را در یک سمت صورت خود دریافت کردند، همراه با یک کرم ۴% HQ که دوبار در روز به طور کامل بر روی صورت اعمال میشد. این مطالعه نیز هیچ تفاوت معنیداری بین درمان ترکیبی و درمان فقط HQ پیدا نکرد.
در مقابل، برخی از مطالعات اثر امیدوارکنندهای از ترکیب لایهبرداری GA با درمانهای موضعی نشان دادهاند. Sakar و همکاران گزارش دادند که بهبودی معناداری در نمرات MASI ۲۱ هفته پس از درمان در گروهی که لایهبرداری GA ۳۰%–۴۰% همراه با TCC دریافت کردند، نسبت به گروه تنها با TCC مشاهده شد. به طور مشابه، در مطالعهای که توسط Dayal و همکاران انجام شد، ترکیب لایهبرداری GA با کرم ۲۰% اسید آزلائیک بهبودی معناداری در نمرات MASI نسبت به گروه فقط موضعی نشان داد. با این حال، باید توجه داشت که در گروه ترکیبی، عوارض جانبی بیشتری مانند اریتم، احساس سوزش و PIH مشاهده شد.
۲) سایر لایهبرداریهای شیمیایی
عوامل مختلفی از جمله SA، TCA و اسید لاکتیک برای لایهبرداری شیمیایی در بیماران مبتلا به ملاسمیا مورد بررسی قرار گرفتهاند. اگرچه شواهدی که از این روشها پشتیبانی کند محدود است، این روشها میتوانند به عنوان یک گزینه برای افرادی که به درمانهای موضعی پاسخ مناسبی ندادهاند، در نظر گرفته شوند.
درمانهای لیزری و نوری
دستگاههای نوری مختلفی در درمان ملاسمیا به کار گرفته شدهاند، که IPL اثربخشی آن را در درمانهای مستقل و ترکیبی نشان داده است، همانطور که توسط چندین مطالعه مقیاس کوچک اشاره شده است. IPL طیف وسیعی از نور (۵۰۰ تا ۱۲۰۰ نانومتر) را منتشر میکند، که آن را برای شرایط مختلف پوستی از جمله اختلالات پیگمنتی مناسب میسازد. در یک مطالعه که توسط Choi و همکاران انجام شد، ۳۰ بیمار آسیایی که درمان با IPL تقسیم شده را در طی ۱۴ هفته دریافت کردند، اثربخشی متوسطی در برابر ملاسمیا نشان دادند. Wang و همکاران اثربخشی IPL را در ترکیب با TCC و ضد آفتاب گزارش کردند و به عدم وجود عوارض جانبی جدی اشاره کردند. علاوه بر این، زمانی که IPL با لیزر روبی QS (QSRL) ترکیب شد، نمرات MASI کاهش یافت و این کاهش در پیگیری ۳ ماهه حفظ شد.
درمان با لیزر، که شامل دستگاههای مختلفی مانند لیزرهای ابلیتیو (از جمله لیزر CO2 و لیزر Erbium:YAG [Er:YAG]) و لیزرهای غیرابلیتیو (مانند لیزر Nd:YAG QS، لیزر روبی QS و لیزر پالس رنگی [PDL]) است، مطالعه گستردهای را پشت سر گذاشته است. با این حال، لیزرهای ابلیتیو مانند لیزر CO2 و لیزر Er:YAG به دلیل احتمال تغییرات رنگدانه پس از درمان، حساستر به نظر میرسند. در مطالعهای که توسط حسن و همکاران انجام شد، بیماران مبتلا به ملاسمیا که درمان با PDL دریافت کردند، اثرات امیدوارکنندهای نشان دادند.
در میان دستگاههای لیزری موجود، لیزر Nd:YAG QS انتخاب ترجیحی است. در گذشته، درمان لیزری برای ملاسمیا به دلیل خطر هیپرپیگمانتاسیون یا هیپوپیگمانتاسیون توصیه نمیشد. با این حال، از زمان معرفی مفهوم “تنینگ لیزری”، لیزرها به طور فزایندهای برای درمان ملاسمیا استفاده شدهاند. تنینگ لیزری شامل اعمال مکرر لیزر Nd:YAG با طول موج ۱۰۶۴ نانومتر با قطر بزرگتر و فلونس پایینتر به نواحی تحت تاثیر ملاسمیا است. این رویکرد درمانی مکرر به دلیل اثربخشی آن در بهبود ملاسمیا محبوب شده است. علاوه بر این، با پسزمینه نظری فتوترمولیز انتخابی زیرسلولی، پزشکان بیشتری این تکنیک را پذیرفتهاند.
کیم و همکاران پیشنهاد دادند که فتوترمولیز انتخابی زیرسلولی به عنوان مکانیسم “تنینگ لیزری” عمل میکند. آنها پس از درمان با EM سهبعدی، کوتاه شدن دندریتهای ملانوستها را مشاهده کردند. با هدفگیری ملانوستها و ملانوزومهای مرحله IV، این درمان لیزری آسیبهای collateral را به حداقل میرساند و یک رویکرد امیدوارکننده برای درمان ملاسمیا با عوارض جانبی کمتر ارائه میدهد. با این حال، لکوسیدرم پونکتو (سفیدی نقطهای پوست) به نگرانی تبدیل شده است و با درمانهای مکرر و پیوسته، منجر به تخریب ملانوستها میشود.
همچنین، توسعه لیزر پیکوثانیهای نیز صورت گرفته است. فنگ و همکاران لیزر Nd:YAG ۱۰۶۴ نانومتر پیکوثانیه و نانوثانیه را در درمان ملاسمیا در یک مطالعه بالینی تقسیم صورت تصادفی مقایسه کردند. آنها نتیجهگیری کردند که اثربخشی در درمان ملاسمیا تقریباً مشابه است. با این حال، لیزر پیکوثانیه درد کمتری در حین انجام درمان داشت و خطر تشدید ملاسمیا را به میزان کمتری داشت.
علاوه بر این، ملاسمیا در حال حاضر به عنوان یک بیماری پیری ناشی از نور (photoaging) در نظر گرفته میشود و روند فزایندهای در ترکیب درمانهایی که هدف آنها درم است، با توجه به تأثیر آن بر ملاسمیا وجود دارد. در این زمینه، دستگاههایی که از منابع انرژی جایگزین استفاده میکنند، مانند دستگاههای رادیوفرکانسی (RF)، نتایج امیدوارکنندهای در درمان ملاسمیا نشان دادهاند. در یک مطالعه، استفاده از RF مونوپولار همراه با اسید کوجیک به بهبود نمرات MASI منجر شد. با این حال، نبود کنترلها تفسیر این نتایج را محدود میکند. میکرونیدلینگ RF، که به دلیل سایش حداقل اپیدرمی شناخته شده است، در احیای پوست مؤثر است و پتانسیل درمان ملاسمیا را از طریق بهبود ECM آسیبدیده و تسهیل حذف ملانین دارد.
تحقیقات اخیر نشان میدهند که میکرونیدلینگ RF نوع پالس میتواند برای ملاسمیای مقاوم به درمان به طور مؤثر استفاده شود، به دلیل اثرات آن، از جمله افزایش نفوذپذیری برای درمانهای موضعی و القای تغییرات مختلف در درم مانند تغییرات در عروق، شستشوی ملانین و نئو کلاژنسازی.
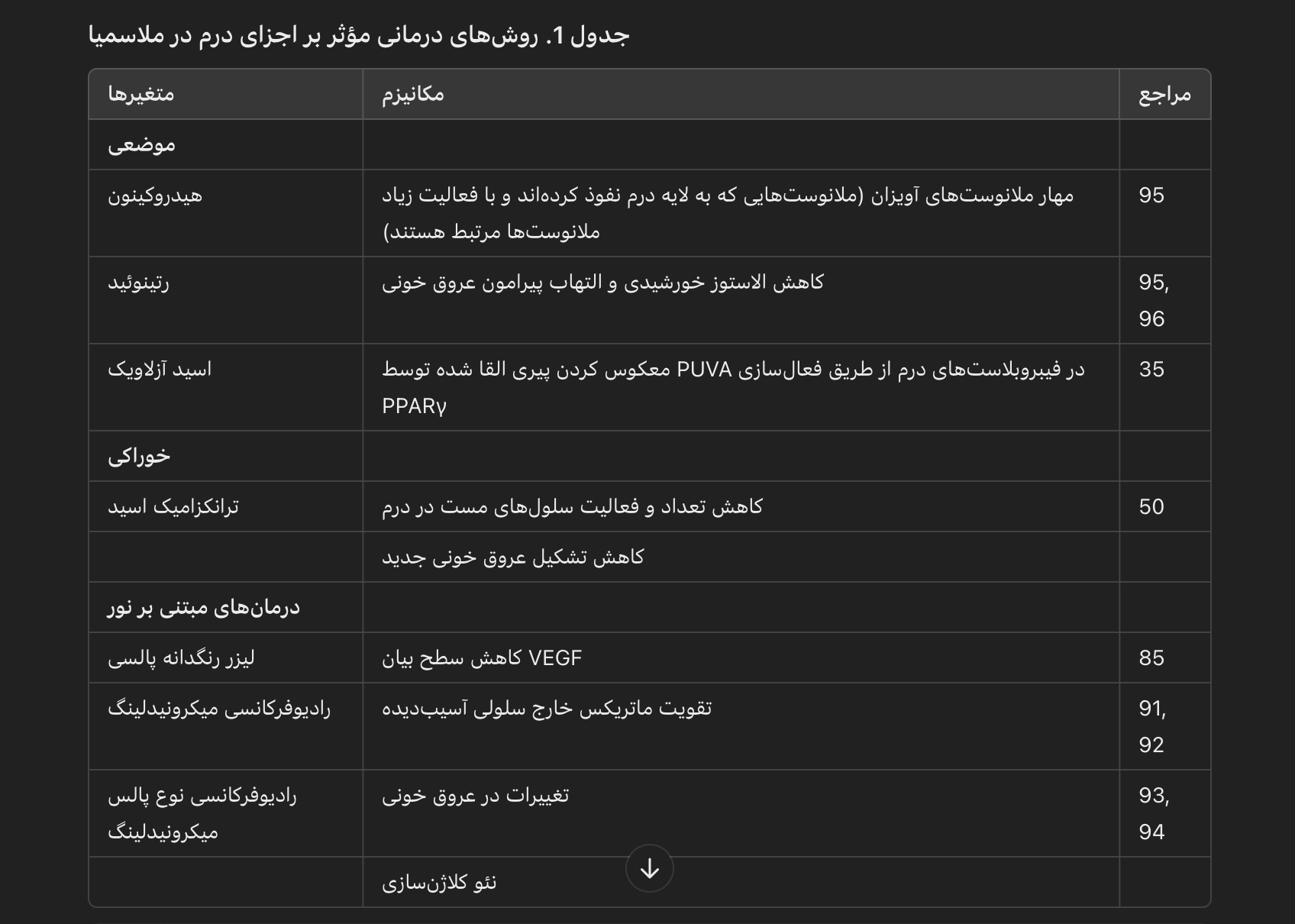
پزشکان باید با دقت شواهد موجود و عوامل خاص بیمار را هنگام انتخاب مناسبترین روش درمانی برای ملاسمیا در نظر بگیرند، به طوری که هم اثربخشی و هم رضایت بیمار در درمان این اختلال رنگدانهای چالشبرانگیز بهبود یابد. در حالی که درمان تکدارویی هیدروکینون و کرم ترکیبی سهگانه هنوز استاندارد طلایی برای درمان ملاسمیا باقی مانده است، با توجه به آسیبهای درم در ملاسمیا و ویژگیهای چالشبرانگیز آن، درمانهای مبتنی بر نور میتوانند به عنوان درمان مکمل در نظر گرفته شوند. در حال حاضر، QSNYL اولین انتخاب در درمان لیزری است، اما برای بیماران مبتلا به ملاسمیای مقاوم، درمانهای مبتنی بر نور که درم پیری شده به هدف قرار میدهند، مانند RF یا PDL، باید در نظر گرفته شوند. روشهای درمانی که بر اجزای درم تاثیر میگذارند، در جدول 1 خلاصه شدهاند.
نتیجهگیری
با توجه به اینکه ملاسما ویژگیهای یک اختلال پیری ناشی از نور خورشید را نشان میدهد، مانند اختلال در غشای پایه، الاستوز خورشیدی، آنژیوژنز و نفوذ سلولهای ماست در درم، اهمیت دارد که هنگام درمان ملاسما، پاتوژنز آن را در نظر بگیریم. انواع مختلفی از سلولها، از جمله ملانوستها، کراتینوسیتها، سبوسیتها، سلولهای ماست و سلولهای اندوتلیال، در ملاسما درگیر هستند. بنابراین، هنگامی که به درمان مؤثر ملاسما میپردازیم، باید ویژگیهای مرتبط با پیری ناشی از نور خورشید را به عنوان اولویت در نظر بگیریم.
در واقع، یک رویکرد درمانی ترکیبی که شامل هر دو جنبه از سفید کردن اپیدرمال و تقویت پیری ناشی از نور خورشید در درم باشد، برای کاهش خطر عود مجدد ملاسما ضروری به نظر میرسد. توسعه مواد سفیدکننده ایمنتر و مؤثرتر، و همچنین عوامل درمانی یا درمانهای مبتنی بر نور که بتوانند اجزای درم را که شامل غشای پایه آسیب دیده یا اجزای درم که به درستی تنظیم نشدهاند، ترمیم کنند، باید توسعه یابد